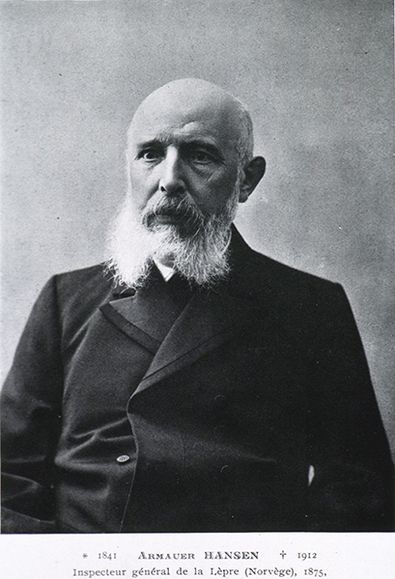Entdecker des Lepra-Erregers
Obwohl Lepra als eine der ältesten Krankheiten der Menschheit gilt, ist sie bis heute kaum erforscht. Der auslösende Krankheitserreger, das Mycobacterium leprae, wurde erst 1879 von dem Norweger Gerhard Armauer Hansen entdeckt. Deshalb wird Lepra auch als Morbus Hansen oder schlicht Hansenkrankheit bezeichnet.
Hansen, mit bürgerlichem Namen Gerhard Henrik Hansen, wurde am 29. Juli 1841 im norwegischen Bergen als achtes der insgesamt 15 Kinder des Ehepaares Claus Hansen und Elizabeth Concordia Schram geboren. Als Kind verbrachte Hansen viel Zeit auf dem Bauernhof seines Onkels. Obwohl die Familie wenig Geld hatte, besuchte Hansen das Gymnasium und begann anschließend an der Königlichen Friedrichs-Universität im heutigen Oslo sein Studium der Medizin, das er 1866 mit Auszeichnung abschloss.
Nach einiger Zeit, in der er als Arzt – unter anderem auf den Lofoten – arbeitete, kehrte er 1868 nach Bergen zurück. Die zweitgrößte Stadt Norwegens galt aufgrund der in Skandinavien steigenden Zahl der Lepra-Erkrankungen damals als Zentrum der europäischen Lepraforschung. Zwischen 1850 und 1900 hatte Bergen drei Leprakrankenhäuser und die größte Konzentration von Lepra-Patient*innen in Europa. Das älteste Leprakrankenhaus der Stadt, das St. Jørgen's Hospital, ist heute nicht nur ein Denkmal für tausende von persönlichen Tragödien, sondern auch ein wichtiger Schauplatz der norwegischen Arbeit und Forschung über Lepra.
Hansen arbeitete damals am Lungegaard-Hospital, einer Forschungseinrichtung unter Leitung von Daniel Cornelius Danielssen mit Platz für 90 Lepra-Patient*innen. Als Danielssens Assistent veröffentlichte Hansen 1869 seine erste Arbeit zur Lepra. Parallel dazu erhielt er für seine Dissertation („Beitrag zur normalen und pathologischen Anatomie der Lymphknoten“) das Stipendium „Professor Skjelderups Goldmedaille für medizinische wissenschaftliche Arbeit“.
Im Gegensatz zu Danielssen, der Lepra als Erbkrankheit betrachtete, tendierte Hansen schnell in Richtung Infektionskrankheit. Um sich auf dem Gebiet der Bakteriologie weiterzubilden, besuchte er 1870 das Anatomische Institut der Universität Bonn, um sich im Mikroskopieren zu üben. Aufgrund des Deutsch-Französischen Krieges sah er sich gezwungen, nach Wien weiterzureisen. Hier kam Hansen erstmalig mit den Lehren Charles Darwins in Berührung, die sein Weltbild nachhaltig verändern und prägen sollten.